Labore für Stabile Isotope (LSI)
Kompetenzzentrum für Isotopenanalytik
Die Labore für Stabile Isotope (LSI) sind ein Zusammenschluss von UFZ-Forschungslaboren, die über eine langjährige Expertise in der Analytik stabiler Isotope (z. B. H, C, N, O, S, Cl) verfügen und damit ein einzigartiges Kompetenzzentrum für Isotopenanalytik bilden. Wir bieten innovative, fortschrittliche Messgeräte und Laborausstattung sowie fachkundige Anleitung und Unterstützung bei der Analyse von Proben. Die hier angewandten Analysetechniken ermöglichen skalenübergreifende Untersuchungen (von Anaylsen auf molekularer Ebene bis hin zu Untersuchungen von z.B. Flusseinzugsgebieten) und werden beispielsweise angewendet im Rahmen von:
- Überwachung biogeochemischer Elementkreisläufe im Rahmen der Anpassung an den Klimawandel, der Energiespeicherung und dem Transport und Umsatz von Schadstoffen/Nährstoffen in terrestrischen und Süßwasser-Ökosystemen
- Charakterisierung des Lebenszyklus von Chemikalien (von der Produktion bis zur Beseitigung und von hochkonzentrierten Altlasten bis zu Mikroverunreinigungen)
- Herkunftsanalyse organischer Materialien und Abschätzung von trophischen Positionen in Nahrungsnetzen
- Beschreibung der Fließwege von Wasser und Berechnung der Verweilzeiten und Altersverteilungen von Wasser und gelösten Stoffen
Service
Unsere Kernkompetenzen sind: (I) on-line bulk sowie der verbindungsspezifischen Isotopenanalyse (BSIA und CSIA), (II) Methodenentwicklung für die Isotopenanalytik von gasförmigen, festen und flüssigen Proben, (III) Qualitätskontrolle und -management für die Analyse stabiler Isotope und (IV) Entwicklung und Kalibrierung internationaler Isotopenreferenzmaterialien.
Wir begrüßen Kooperationen zur Erweiterung und Verbesserung der Anwendbarkeit der Stabilisotopenanalytik. Eine Liste der verfügbaren Instrumente und möglichen Anwendungen finden Sie unten. Wenn Sie Fragen zur Anwendung von stabilen Isotopen in Ihren Experimenten oder zur Analyse Ihrer Proben haben, setzen Sie sich gerne mit uns in Verbindung.
Verfügbare Instrumente für die Analyse stabiler Isotope
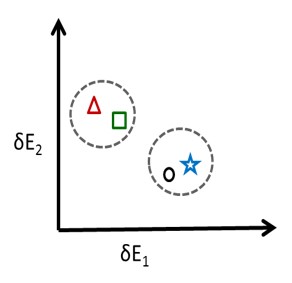
Fragen, die beantwortet werden sollen:
Woher stammt die Verbindung?
Welche Stellung nehmen spezifische Arten in Nahrungsnetzen ein?
Wie lassen sich vergangene Umwelt- und Klimabedingungen rekonstruieren?
Wie kann man Lebensmittelproben authentifizieren?
Was ist das Isotopenverhältnis eines Referenzmaterials, das für die verbindungsspezifische Analyse stabiler Isotope verwendet wird? ...
Wie geht man vor:
Bestimmung des C-, N- und/oder S-Stabilisotopenverhältnisses einer Probe mittels Elementaranalysator-Isotopenverhältnis-Massenspektrometrie (EA-IRMS) oder Bestimmung des H- und/oder O-Stabilisotopenverhältnisses einer Probe mittels Hochtemperatur-Konversions-Isotopenverhältnis-Massenspektrometrie (HTC-IRMS).
Anforderungen an die Probe:
Die Probe kann organisch oder anorganisch, fest oder flüssig, in natürlicher Häufigkeit oder isotopisch angereichert sein.
Beispiele aus der Literatur:
Organic reference materials for hydrogen, carbon, and nitrogen stable isotope-ratio measurements: Caffeines, n-alkanes, fatty acid methyl esters, glycines, l-valines, polyethylenes, and oils. Schimmelmann, A., Qi, H., Coplen, T.B., et al. Analytical Chemistry. 88, 4294-4302 (2016).
Multidimensional isotope analysis of carbon, hydrogen and oxygen as tool for identification of the origin of ibuprofen. Gilevska, T., Gehre, M. & Richnow, H.H. Journal of Pharmaceutical and Biomedical Analysis. 115, 410-417 (2015).
Using Stable Isotopes to estimate Trophic Position: Models, Methods, and Assumptions.
Post, D.M. Ecology 83, 703-718 (2002).
Kontakt
Dr. Steffen Kümmel
steffen.kuemmel@ufz.de
+49 (0) 341 6025 1362
Dr. Mario Brauns
mario.brauns@ufz.de
+49 (0) 391 6025 9140
Dr. Kay Knöller
kay.knoeller@ufz.de
+49 (0) 341 6025 4444
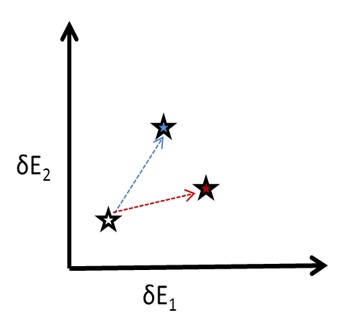
Fragen, die beantwortet werden sollen:
Wie lassen sich dynamische Prozesse (z.B. der biologische Abbau von Chemikalien) visualisieren?
Wie lassen sich Prozesse unterscheiden, die auf dieselbe Verbindung einwirken?
Wie lassen sich Umwandlungsprozesse qunatifizieren? ...
Wie geht man vor:
Bestimmung der stabilen C-, N-, und/oder H-Isotopenverhältnisse einer Probe mittels Gaschromatographie - Isotopenverhältnis-Massenspektrometrie (GC-IRMS) oder Bestimmung der stabilen Cl- und/oder S-Isotopenverhältnisse (δ34S, δ33S) einer Probe mittels Gaschromatographie - multi-Kollector - induktiv gekoppeltes Plasma-Massenspektrometrie (GC-MC-ICPMS).
Anforderungen an die Probe:
Die Probe muss organisch sein, kann aber flüssig oder gasförmig sein. Darüberhinaus kann die Probe eine natürliche Isotopenhäufigkeit aufweisen oder isotopisch angereichert sein.
Beispiele aus der Literatur:
Investigation of active site amino acid influence on carbon and chlorine isotope fractionation during reductive dechlorination. Phillips, E., Bulka, O., Picott, K., et al. FEMS Microbiology Ecology. 98, fiac072 (2022).
Photosynthesis-driven methane production in oxic lake water as an important contributor to methane emission. Günthel, M., Klawonn, I., Woodhouse, J. et al. Limnology and Oceanography. 65, 2853-2865 (2020).
Distinct carbon isotope fractionation signatures during biotic and abiotic reductive transformation of chlordecone. Chevallier, M.L., Cooper, M., Kümmel, S., et al. Environmental Science and Technology. 52, 3615-3624 (2018).
Triple-element compound-specific stable isotope analysis of 1,2-dichloroethane for characterization of the underlying dehalogenation reaction in two Dehalococcoides mccartyi strains. Franke, S., Lihl, C., Renpenning, J., et al. FEMS Microbiology Ecology. 93 fix137 (2017).
Kontakt
Dr. Steffen Kümmel (Leipzig)
steffen.kuemmel@ufz.de
+ 49 (0) 341 6025 1362
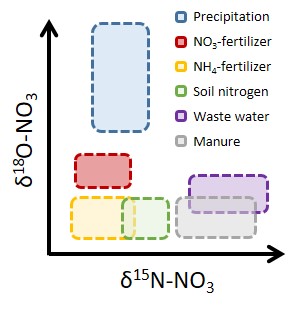
Fragen, die beantwortet werden sollen:
Welche Quellen tragen zu einem Pool an gelösten Stoffen bei?
Welche physikalischen und (bio)chemischen Prozesse beeinflussen einen Pool an gelösten Stoffen (z.B. Verdünnung, Durchmischung, natürlicher und stimulierter bakterieller Umsatz,...)?
Wie hoch ist die absolute Menge und Geschwindigkeit des Stoffumsatzes? ...
Wie geht man vor:
Bestimmung der stabilen C-, N-, O- und/oder S-Isotopenverhältnisse von gelösten Stoffen in einer Probe durch eine Abfolge von chemischen Präparations- und Isotopenanalysetechniken (z. B. Gasisotopenverhältnis-Massenspektrometrie, Elementaranalyse, Hochtemperaturpyrolyse, 'Off-Axis Integrated Cavity Output' Spektroskopie, Denitrifikationsmethode).
Anforderungen an die Probe:
Die Wasserprobe oder des auslaugbaren Feststoffs muss eine ausreichende Menge des gelösten Stoffs enthalten (z. B. Nitrat, Nitrit, Ammonium, Sulfat, Phosphat, Bikarbonat).
Beispiele aus der Literatur:
New Ag3PO4 comparison material for stable oxygen isotope analysis.
Watzinger, A., Schott, K., Hood‐Nowotny, R., et al. Rapid Communications in Mass Spectrometry. 35, e9101 (2021).
High spatial-resolution monitoring to investigate nitrate export and its drivers in a mesoscale river catchment along an anthropogenic land-cover gradient. Bujak, I., Müller, C., Merz, R., et al. Hydrological Processes. 35, e14361 (2021).
Tomography of anthropogenic nitrate contribution along a mesoscale river. Müller, C., Musolff, A., Strachauer, U., et al. Science of the Total Environment. 615 (2018).
Kontakt
Dr. Kay Knöller (Halle/Saale)
kay.knoeller@ufz.de
+49 (0) 341 6025 4444
Dr. Christin Müller (Halle/Saale)
christin.mueller@ufz.de
+49 (0) 341 6025 4235
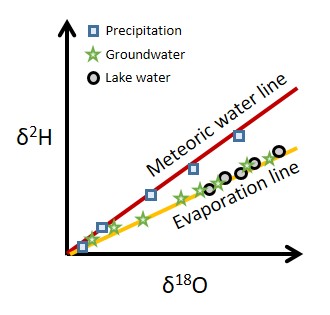
Fragen, die beantwortet werden sollen:
Woher kommt das Wasser?
Welches sind die vorherrschenden Bewegungspfade von Wasser und Wasserdampf in aquatischen und atmosphärischen Systemen über verschiedene Skalen hinweg?
Wie interagieren verschiedene Kompartimente in aquatischen Systemen?
Wie wirken sich extreme hydrologische Ereignisse auf die Fließwege und Laufzeiten von Wasser und gelösten Stoffen aus? ...
Wie geht man vor:
Bestimmung des Verhältnisses der stabilen Isotope von O und/oder H in einer Wasserprobe mittels Laser-Cavity-Ringdown-Spektroskopie.
Verwendung eines automatischen Hochfrequenz-Probenehmers, der für die Sammlung von Proben stabiler Isotope spezifiziert sind.
Anforderungen an die Probe:
Die Wasserprobe muss ein Mindestvolumen von 5 mL haben und gefiltert sein. Die Probe kann manuell oder mittels eines Hochfrequenz-Autosampler gesammelt werden.
Beispiele aus der Literatur:
Upscaling Tracer-Aided Ecohydrological Modeling to Larger Catchments: Implications for Process Representation and Heterogeneity in Landscape Organization
Yang, X., Tetzlaff, D., Müller, C., et al. Water Resources Research. 59, e2022WR033033 (2023).
Technical note: A microcontroller-based automatic rain sampler for stable isotope studies. Michelsen, N., Laube, G., Friesen, J., et al. Hydrology and Earth System Sciences. 23, 2637-2645 (2019).
Kontakt
Dr. Kay Knöller (Halle/Saale)
kay.knoeller@ufz.de
+49 (0) 341 6025 4444
Christina Radtke (Halle/Saale)
christina.radtke@ufz.de
+49 (0) 341 6025 4192
Dr. Christin Müller (Halle/Saale)
christin.mueller@ufz.de
+49 (0) 341 6025 4235
Informationen über die Anwendung der Analytik stabiler Isotope in den Naturwissenschaften:
Isotopic composition of nitrogen species in groundwater under agricultural areas: A review.
Nikolenko, O., Jurado, A., Borges, A.V., et al. Science of the Total Environment. 621, 1415-1432 (2018).
On the use of stable isotopes in trophic ecology.
Boecklen, W.J., Yarnes, C.T., Cook, B., et al. Annual Review of Ecology, Evolution, and Systematics. 42:1, 411-440 (2011).
Principles and Mechanisms of Isotope Fractionation. Hunkeler, D. & Elsner, M. In Environmental Isotopes in Biodegradation and Bioremediation, Taylor & Francis Group, Boca Raton, FL (2010).
Informationen über Geräte für die online bulk und verbindungsspezifische Analyse stabiler Isotope:
Perspectives of compound-specific isotope analysis of organic contaminants for assessing environmental fate and managing chemical pollution.
Hofstetter, T.B., Bakkour, R., Buchner, D., et al. Nature Water. 2, 14-30 (2023).
A review on environmental isotope analysis of aquatic micropollutants: Recent advances, pitfalls and perspectives.
Blessing, M. & Baran, N. Trends in Analytical Chemistry. 157, 116730 (2022).
Recent advances in multi-element compound-specific stable isotope analysis of organohalides: Achievements, challenges and prospects for assessing environmental sources and transformation. Nijenhuis, I., Renpenning, J., Kümmel, S., et al. Trends in Environmental Analytical Chemistry. 11, 1–8 (2016).
Netzwerke und weitere Aktivitäten
Das halbjährlich stattfindende UFZ - Isotopenplattformtreffen soll aktuelle und potenzielle zukünftige Nutzer der Stabilisotopenanalytik zusammenbringen. Ein zentrales Element des Treffens sind Präsentationen über neue Möglichkeiten und Anwendungen der Stabilisotopenanalytik im Kontext der UFZ-Forschung. Darüber hinaus können zukünftige Bedürfnisse und Interessen der UFZ-Forscher diskutiert werden.
Bitte kontaktieren Sie uns, wenn Sie Interesse an einer Teilnahme am Isotopenplattformtreffen haben.
Kontakt
Dr. Steffen Kümmel
steffen.kuemmel@ufz.de
+ 49 (0) 341 6025 1362
Wir bieten Kurse an, die einen Überblick über Konzepte der stabilen Isotope geben. Dies reicht von der Bewertung biogeochemischer Prozesse einschließlich der Aufnahme, des Transports und der Umwandlung von Chemikalien in mikrobiellen Kulturen, in komplexen mikrobiellen Gemeinschaften (einschließlich Zell-Zell-Interaktionen) bis hin zu Umweltprozessen auf der Ebene von Flusseinzugsgebieten. Die beiden wichtigsten prinzipiellen Ansätze, die stabile Isotope in ihrer natürlichen Häufigkeit oder angereichert als Tracer nutzen, werden mit spezifischen Konzepten, der entsprechenden Ausrüstung und Anwendungsbeispielen vorgestellt. Zusätzlich werden derzeit spezielle Kurse in Erwägung gezogen.
Bitte setzen Sie sich mit uns in Verbindung, wenn Sie an einem Kurs über Konzepte oder Methoden zur Stabilisotopenanalytik interessiert sind.
Kontakt
Dr. Ivonne Nijenhuis
ivonne.nijenhuis@ufz.de
+49 (0) 341 6025 1356
Die LSI arbeiten mit zahlreichen nationalen und internationalen Partnern zusammen. Die Expertise des LSI wird in einer Vielzahl von Prozessstudien sowie in Projekten zur Qualitätskontrolle und Qualitätssicherung in der stabilen Isotopenanalyse in Zusammenarbeit mit folgenden Partnern angewendet:
International Atomic Energy Agency (IAEA)
National Institute for Standards and Technology (NIST)







